消毒剂和免洗消毒洗手液出口美国,需要做好这些准备工作?
经过全国人民一个多月的同舟共济,艰苦奋战,国内的疫情终于逐渐缓解。
然而,新冠病毒却开始在全球肆虐。
世界卫生组织总干事谭德塞于11日表示,新冠肺炎疫情已具有全球大流行特征,但这也是历史上第一个可以控制的大流行病。
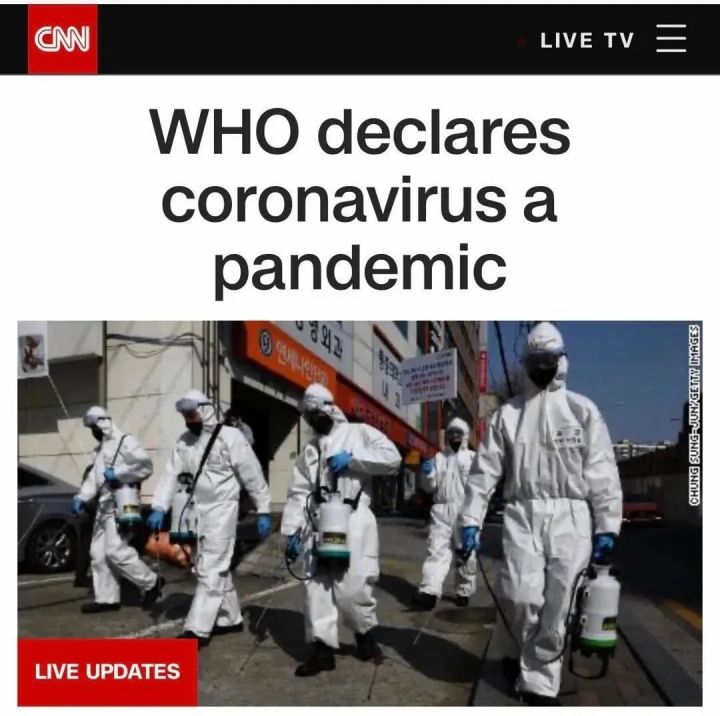
预防新型冠状病毒,除了有效的隔离, 正确的消毒也是极其重要的一项控制措施。
欧美国家虽然一直不承认口罩的有效性,但都一致认可洗手或者手部消毒是很有效的方法。
同时也说明,免洗消毒洗手液这类产品已经开始在各个国家断供。
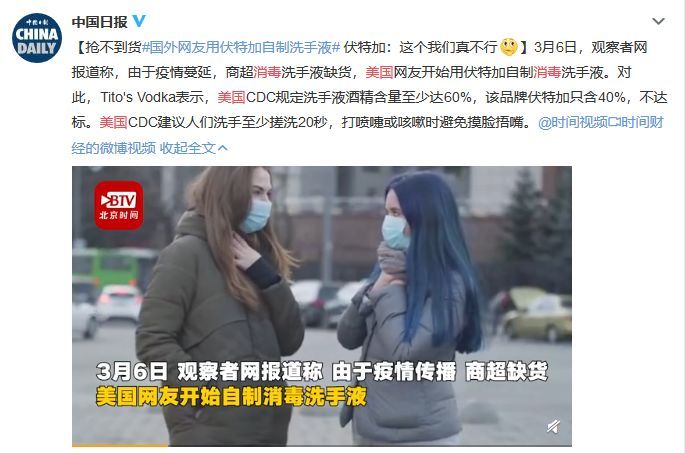
为了让更多合规的消毒剂产品可以顺利进入需求市场瑞欧科技近期一直在关注各个国家和地区对消毒剂的上市规定,今天,我们主要了解下免洗消毒洗手液,出口美国的具体要求。
免洗消毒洗手液出口美国的要求
在美国,免洗消毒洗手液属于局部消毒的非处方药(OTC, Over-the-Counter),与去屑洗发水、含氟牙膏、防晒霜等产品一样,受食品药品监督管理局(FDA)监管。
虽然属于药品类,但大部分OTC产品的合规要求还是比较简单的。
一般来说,FDA会统一审查用于OTC药品的活性成分,并最终出具一份OTC 专论(OTC Monograph)。
OTC专论就相当于活性物质标准,对于OTC产品,只要其中的活性成分满足OTC专论的要求,就可以不经FDA审批直接上市。
需要注意,不用FDA审批并不意味着OTC药品上市没有任何合规义务,产品仍旧需要满足一定的要求,具体的要求如下:
1、OTC药品里的活性成分必须有现成的OTC专论,并且企业所用的活性成分符合OTC专论的要求,否则产品就要做OTC新药申请;对含酒精的免洗消毒洗手液来说,酒精在美国已经有相应的OTC专论,所以只要用于生产的酒精满足专论的要求,产品上市就可以不用经过FDA审批了。
2、OTC药品的生产商或进出口商必须进行FDA厂址登记,对美国境外的企业来说,则需要委托美国境内的代理进行FDA厂址登记。
3、为OTC药品申请一个国家药品编号(NDA, National Drug Code)。
4、企业必须把将要进入美国市场的所有OTC药品列出清单并在FDA进行备份,之后此清单每年至少要在6月和12月更新两次。
5、OTC药品的标签必须符合相应的标签规定
6、生产工厂必须满足动态药品生产管理规范(cGMP)的要求
总体来看,对于生产工厂已经满足cGMP要求的企业来说,剩下的5项合规义务都比较简单
瑞欧与您共尽绵薄之力
瑞欧科技在美国设有独立的子公司,可以作为广大企业的美国代理商,协助广大企业完成FDA机构登记及其他合规相关事宜,整个合规流程所需要的时间会在一个月左右。
当前全球正在遭受新型冠状病毒的侵害,疫情形势严峻,瑞欧科技始终愿用我们的专业能力,为这场病毒战役尽绵薄之力。
我们深耕欧盟、美国、中国消毒剂合规领域多年,拥有专业的技术团队和丰富的申报经验,助力消毒剂企业顺利进入需求市场,希望以此能帮助全球人民有更多消毒剂产品选择和使用,一起共度疫情难关!